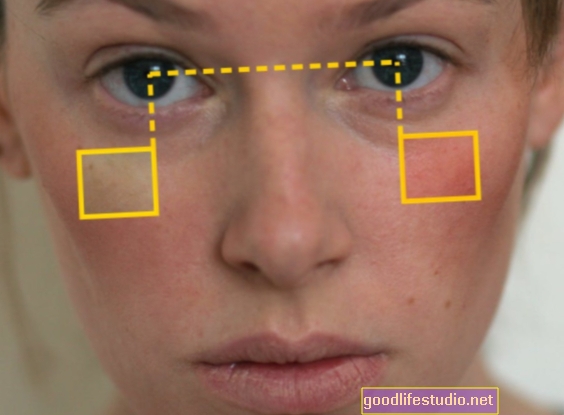
Az ólomnak a prenatális idegfejlődés veszélye


A prenatális időszakban a magzat a természet egyik legösszetettebb struktúráját, az emberi agyat kezdi kialakítani. Ezt a folyamatot idegi embriogenezisnek hívják, és a prenatális élet egyik legbonyolultabb folyamatát képviseli. A folyamat az agyat alkotó sejtek viselkedésének szigorú szabályozásán alapul. A neuronális őssejtek (NSC) kulcsszerepet játszanak az embrionális agy fejlődésében.
Az NSC-knek különleges környezetre van szükségük ahhoz, hogy képesek legyenek ellátni funkciójukat az idegi embriogenezisben, új sejtek létrehozásában az idegrendszer népesítésére. Bizonyos esetekben azonban a káros környezeti expozíció rendellenes NSC viselkedést eredményezhet. A prenatális ólomnak való kitettség egyike ezeknek a káros hatásoknak, amelyek felülmúlhatják az NSC-k mechanizmusait a sejtkárosodás kezelésében. Ennek eredményeként az NSC által szabályozott folyamatok az idegi embriogenezisben érintettek lehetnek, amelyek gyakran neurodevelopmentális rendellenességekhez vezetnek.
Megtermékenyítéskor egyetlen sejtből sejttömeg alakul ki, majd később ez a tömeg több rétegre oszlik, amelyekből az emberi test összes szerkezete származik. Ez a központi idegrendszer esetében is érvényes. Az egyik rétegből származik, amely az idegcsövet alkotja, az agy, az agytörzs és a gerincvelő prekurzorát. Kezdetben az idegcső meglehetősen kicsi, de az NSC-kből új sejtek létrehozása miatt fokozatosan megnő. Később az idegcsőben lévő sejtek különféle funkciókra specializálódnak, megváltoztatva sejtes és biokémiai jellemzőiket. Nyilvánvaló, hogy ha a fenti lépések bármelyikén elromlik valami, akkor fejlődési agyi rendellenességek léphetnek fel.
Az ólom hosszú ideig az emberi civilizáció része volt. Azonban csak nemrégiben kezdtek megjelenni azok a mechanizmusok, amelyek révén az ólom negatív egészségügyi hatásokat okoz. Az ólom különösen káros az NSC-k számára, még akkor is, ha az expozíció minimális. Az ólomnak a születés előtti nagyon minimális expozíciója alacsonyabb IQ-val, agresszivitással és más problémákkal függ össze. Kutatási tanulmányok azt is kimutatták, hogy a prenatális ólomnak való kitettség több kárt okoz, mint a posztnatális időszakban történő kitettség. Ezeket a megállapításokat összekapcsolják az NSC-k ólom általi sejtsérülésének mechanizmusaival. A javasolt mechanizmusok befolyásolják az alapvető sejtfunkciókat, amelyek a reaktív oxigénfajok (ROS) növekedését és a DNS-metiláció változását eredményezik.
A reaktív oxigénfajok olyan molekulák, amelyek a sejtek légzése következtében természetesen előfordulnak. A kóros körülmények között azonban szintjük jelentősen megemelkedhet. A krónikus ólommérgezés az ROS növekedését eredményezi több mechanizmus révén. Közülük az ólomionoknak közvetlen hatása van a ROS-szintet szabályozó fehérjékre. Ezenkívül az ólom közvetetten növelheti a ROS szintjét az aminolevulinsavval, a hemoglobin komponenseinek biokémiai prekurzorával való kölcsönhatás révén. A ROS károsíthatja a sejt különböző struktúráit, és közben még több ROS-t hozhat létre. Ezenkívül az ROS részt vesz a sejthalál jelzésében és más sejtes válaszokban.


A DNS-metiláció a génexpressziót szabályozó mechanizmusok egyike, a génexpresszió szabályozása pedig a sejtos differenciálódás egyik alapja. Kimutatták, hogy az ólomnak való kitettség megváltoztatja a DNS metilációját, ami viszont az NSC-k differenciálódásának gátlásával jár. Az ólom még nem ismert mechanizmusok révén a metilációs minták változását idézi elő az idegsejtek differenciálódásával szorosan összefüggő gének közelében.
A sejtek nem maradnak passzívak ezekben a folyamatokban. A többi sejthez hasonlóan az NSC-k is rendelkeznek olyan mechanizmussal, amellyel számos ilyen káros eseményt képesek ellensúlyozni. Az egyik legfrissebb vizsgálat az Nrf2 fehérjét érintő folyamatot vizsgálta.
Az Nrf2 közvetlenül kapcsolódik az NSC védelmi mechanizmusához az ólomnak való kitettség okozta oxidatív stressz ellen. Az Nrf2 a citoplazmában található KEAP1 fehérjéhez kapcsolódik. Amikor az ROS szintje megnő, az Nrf2 elválik a KEAP1-től, vándorol a sejtmagba és kötődik az antioxidáns válaszelemeknek (ARE) nevezett specifikus DNS-régiókhoz.Az Nrf2 megkötése után az ARE-k aktiválják a sejtek ROS-méregtelenítéséért felelős különféle fehérjéket kódoló célgének expresszióját.
Ezenkívül egy új Nrf2 célpontot, az SPP1 fehérjét azonosítottak a közelmúltban. Az SPP1-nek különös jelentősége van az NSC elváltozásában, mivel in vitro vizsgálatok és a kódoló génszekvenciájában lévő mutációk neurológiai betegségekkel való társítása révén neuroprotektív tulajdonságokkal társul. Ezek a hatások egy anti-apoptotikus és pro-proliferatív folyamatot magában foglaló jelátviteli mechanizmus eredménye. A folyamat kompenzációs válaszokat eredményez az NSC-k proliferációjának ólomgátlására. Ennek eredményeként az SPP1-t javasolták az ólom-expozíció neurotoxicitásának védő mediátoraként.
Számos betegség következménye a túlzott sejtkárosodás, amelyhez a sejtek nem képesek alkalmazkodni. Ez vonatkozik azokra az NSC-kre, ahol az esszenciális neurodevelopmentális folyamatok megváltozhatnak az ólom toxicitásával. Bár az NSC-k védelmi mechanizmusokkal vannak felszerelve, gyakran nem elég erősek ahhoz, hogy ellensúlyozzák a káros környezeti hatásokat. Ilyen esetekben az idegi embriogenezis, a szaporodás és a differenciálódás megváltozása történik. A konkrét neurológiai megnyilvánulásokhoz vezető specifikus változásokat még mindig részletesen meg kell vizsgálni.
Az ólom prenatális idegfejlődésre gyakorolt káros hatásának jobb megértése fokozott figyelmet igényel, hogy elkerüljük a jövő anyáinak ennek a toxikus elemnek való kitettségét. Úgy gondolják, hogy terhes nők milliói világszerte rendszeresen ki vannak téve az ólom magas koncentrációjának az élelmiszerekben és az ivóvízben. Ez gyakran befolyásolja a fiatal generáció egészségét a világ számos országában.
Hivatkozások
Peter J. Wagner, Hae-Ryung Park, Zhaoxi Wang, Rory Kirchner, Yongyue Wei, Li Su, Kirstie Stanfield, Tomas R. Guilarte, Robert O. Wright, David C. Christiani és Quan Lu (2016) In Vitro Effects of Ólom a neurális őssejtek génexpressziójáról, valamint a szabályozott gének és a gyermekek kognitív pontszámai közötti asszociációkról. Környezetvédelmi szempontok; DOI: 10.1289 / EHP265
Temple S. (2001) Az idegi őssejtek fejlődése. Nature 414 (6859): 112-7. DOI: 10.1038 / 35102174
Senut MC, Sen A, Cingolani P, Shaik A, Land SJ, Ruden DM (2014) Az ólom-expozíció megzavarja a globális DNS-metilációt az emberi embrionális őssejtekben, és megváltoztatja azok neuronális differenciálódását. Toxicol Sci. 139 (1): 142-61. DOI: 10.1093 / toxsci / kfu028
Seiji Ishii és Kazue Hashimoto-Torii (2015) A prenatális környezeti stressz hatása a kortikális fejlődésre. Elülső. Sejt. Neurosci. 9: 207. DOI: 10.3389 / fncel.2015.00207
Ez a vendégcikk eredetileg a díjnyertes egészségügyi és tudományos blogon és agyi témájú közösségen, a BrainBlogger oldalán jelent meg: Hogyan eredményezi a prenatális ólom expozíció neurodevelopmentális rendellenességeket.