A leukémia agyi hatásait a gének támasztják alá
Néhány akut limfoblasztos leukémia (ALL) miatt kezelt gyermeknél agyi rendellenességek alakulnak ki, és ennek kockázata bizonyos génekhez köthető.
Az ALL a gyermekkorban a leggyakoribb rák, és a betegek mintegy 90 százaléka életben marad. De a kezelés, amely általában kemoterápiát is magában foglal, és magában foglalhatja a koponyasugárzást, hosszú távú problémákat okozhat a memóriában, a tanulásban vagy más kognitív funkciókban.
A memóriazavar különösen meggyengítő tünet, mivel a memória játszik központi szerepet a mindennapi életben, valamint a tanulmányi vagy szakmai sikerekben.
Deborah Waber, Ph.D. és munkatársai a bostoni Gyermekkórházban (Massachusetts, USA) négy specifikus génváltozatot találtak, amelyek a jelek szerint növelik a kockázatot. Ezek a változatok összefüggenek az agy gyulladásával és a sejtek reakciójával az oxidatív stressz okozta károsodásokra, például a kemoterápia által okozott sejtkárosodásra.
Tárolt vérminták és kognitív funkcióteszt eredményei alapján tették meg a feltárást 350 amerikai, USA-ból és Kanadából származó túlélőn. A kognitív tesztek IQ-t, memóriát, figyelemtartományt és hiperaktivitási magatartást tartalmaztak.
A négy kiemelt gén, a NOS3, az SLCO2A1, a HFE és a COMT, egy 28 vizsgált gén csoportjába tartozott a gyógyszer-anyagcserében vagy a sejtkárosító válaszokban betöltött szerepük miatt.
E négy csoport specifikus változatai „szignifikánsan kapcsolódtak a neurokognitív hatásokhoz” - írja a csapat. Mindegyik részt vesz az agy gyulladását szabályozó utakban, vagy megvédi a sejteket az oxidatív stressztől.
Waber elmondta: „Célunk, hogy azonosítani tudjuk, kit fenyeget a késői kognitív hatás, és neuroprotektív beavatkozásokat biztosítani. Ez a retrospektív elemzés azt mondja nekünk, hogy a továbbiakban érdemes lehet megvizsgálnunk a gyermekek genotípusait a kiinduláskor, és prospektív kutatásokat folytatnunk annak megismerése érdekében, hogy ezek a specifikus génvariánsok miért növelhetik a toxicitás kockázatát. "
A tanulmány eredményeit az Amerikai Hematológiai Társaság 56. éves találkozóján mutatták be, amelyet 2014 decemberében tartottak. A csapat reméli, hogy lehetővé válik MINDEN beteg genomikus átvilágítása a hosszú távú memória, figyelem és tanulási hatások kockázata szempontjából.
A vezető szerző, Peter Cole, MD azt mondta: "Minél jobban nézünk ki, annál inkább azt tapasztaljuk, hogy sok túlélő tapasztalja a gondolkodásmód változását. Ha minden ÖSSZES betegnek azonos kezelést adunk, miért van az, hogy néhányuk memória- vagy kognitívhiányt tapasztal, de nem mindegyik?
"Olyan változatokra szorítkoztunk, amelyek a lakosság legalább 10 százalékában vannak jelen, és úgy döntöttünk, hogy érdekel bennünket, hogy elmagyarázzuk, mi történhet a legtöbb betegnél."
A jelentős eredmények ellenére Cole hozzáteszi, hogy további munkálatokra van szükség a négy gén szerepének megerősítéséhez. Egy prospektív vizsgálat, amelyben a betegek génjeit a kezelés előtt tesztelik, megbízhatóbb bizonyítékot szolgáltatna.
Ezenkívül minden védőintervenciót preklinikai és klinikai vizsgálatnak kell alávetni annak biztosítása érdekében, hogy a kezelés sikere ne sérüljön.
Társszerző, Lewis Silverman, MD elmondta: „A gyermekkori ALL klinikai kutatások egyik legfontosabb prioritása a kezelés toxicitásának csökkentése, és minden bizonnyal szeretnénk csökkenteni a késői neurokognitív hatásokat, ha lehetséges.
„Remélhetőleg ez a munka egy olyan módszer felkutatásához fog vezetni, akiknél a legnagyobb a késői neurokognitív hatások kockázata, és akikben összpontosíthatjuk kutatási erőfeszítéseinket, kezelési megközelítésünket módosíthatjuk vagy új védelmi stratégiákat tesztelhetünk a hatások csökkentése céljából anélkül, hogy hátrányosan befolyásolnánk az esélyt gyógyításra. ”
Waber hozzátette, hogy az ALL kezelés agyi hatásával kapcsolatos munkája tíz együttműködő intézményre terjed ki Észak-Amerikában. Korai tanulmányai rámutattak arra, hogy jelentős kognitív hatások vannak az ALL-ben sikeresen kezelt gyermekek körében, és kimutatták, hogy „drámai nemi különbség van, a nők sokkal érzékenyebbek a toxicitásra”.
A gyermek onkológusok régóta keresnek kevésbé toxikus terápiákat. "A dózis csökkentése vagy a koponya sugárzásának megszüntetése a kognitív eredmények jelentős javulását eredményezte, különösen a nők esetében" - mondta Waber.
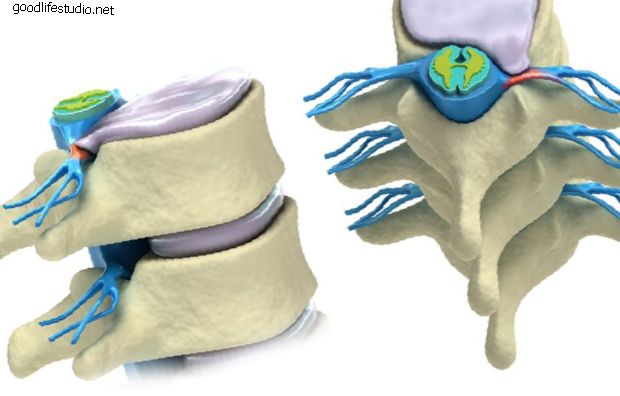
A jelenlegi munka azokra az agyterületekre összpontosul, amelyek a legnagyobb kárt mutatják. Waber elmondta: "A hippokampusz központi szerepet játszik az epizodikus memória kódolásában, és rendkívül érzékeny a kemoterápiára és a sugárterápiára."
A memória kódolásának és tanulásának hiánya, a munkamemória, a figyelem, az információfeldolgozási sebesség és a vizuális térbeli készségek „neuroanatómiailag lokalizálódnak a hippokampuszban a mediális temporális lebenyekben és a frontális lebenyekben”.
A sugárzás és a kemoterápia károsítja a hippokampus idegi őssejtjeit és prekurzor sejtjeit, akadályozva azok megújulását és visszatartva a mielinációt, ami az a létfontosságú folyamat, amelyben az agysejtek olyan szigetelő köpenyt növesztenek, amely felgyorsítja az agyi jeleket, és körülbelül 30 éves korukig nem teljesen teljes. primer agydaganatok és leukémia miatt kezelt egyének postmortememeiben.
"Összefoglalva" - zárta le Waber - ezek a megállapítások funkcionális és strukturális alapot nyújtanak a kognitív tünetek némelyikéhez, amelyet a gyermekkori leukémia túlélői tapasztalnak. "
Referencia
A próba az American Society of Hematology éves találkozójának 56. éves ülésén számolt be, amelyet 2014. december 6–9-én tartottak a Moscone Centerben, San Francisco, Kalifornia.







-treatment.jpg)











.jpg)